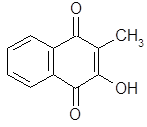
Биологи осваивают сингулярности
Повышение скорости фиксации атомно-молекулярных трансформаций позволит быстрее создавать новые лекарства. Сегодня речь идет о чтении одиночных цепей ДНК, для чего их пропускают сквозь поры.
Создан биоробот из клеток взрослого человека
Андроботы способны регенерировать даже нервные волокна. Преимущество новой технологии в том, что андроботы делаются из собственных клеток человека, это снимает опасность их отторжения иммунной системой.
Таблица 2
Биологическая активность витаминов группы К
Витамины
Активность, %
Витамины
Активность, %
К1
100
К5
100
К2
60
К6
100
К3
300
К7
100
К4
200
Как видно из данных табл. 2, гидрирование хиноидных групп, находящихся в положении 1,4, не оказывает существенного влияния на биологическую активность витаминов К. В то же время гидрирование самого нафтохинонового ядра приводит к почти полной утрате биологической активности молекулы. Замена гидроксильной группы на аминогруппу не сопровождается утратой биологической активности витамина. Для проявления биологической активности обязательно наличие метильной группы в положении 2 нафтохинонового ядра. Введение метильной группы в других позициях нафтохиноновой системы сопровождается резким уменьшением физиологической роли соединения.
Представляет особый интерес влияние изменения длины боковой изопреноидной цепи на биологическую активность производных нафтохинонов. Оказывается, что как укорочение, так удлинение углеводородной цепи вызывает снижение витаминной активности препарата. Наряду с этим полное удаление боковой цепи увеличивает активность молекулы в три раза.
Введение гидроксильных групп в различные позиции нафтохинонового ядра, за исключением положений 1 и 4, почти полностью лишает соединения витаминной активности. Примером 'такого соединения является фтиокол, или 2-метил-З-гидрокси-11,4-нафтохинон:
|
|
|
Фтиокол |
Это соединение почти не обладает К-витаминной активностью, по данным некоторых ученых даже имеет антивитаминные свойства. Некоторые химические соединения, имеющие отдельные черты сходства в строении с витаминами группы К, обладают антивитаминными свойствами. Одним из первых антивитаминов К был открыт дикумарол – вещество, выделенное из испорченного сена бобовых растений (донник, клевер):
|
Перейти на страницу:
1 2 Copyright © 2026 - All Rights Reserved - www.fullbiology.ru
|